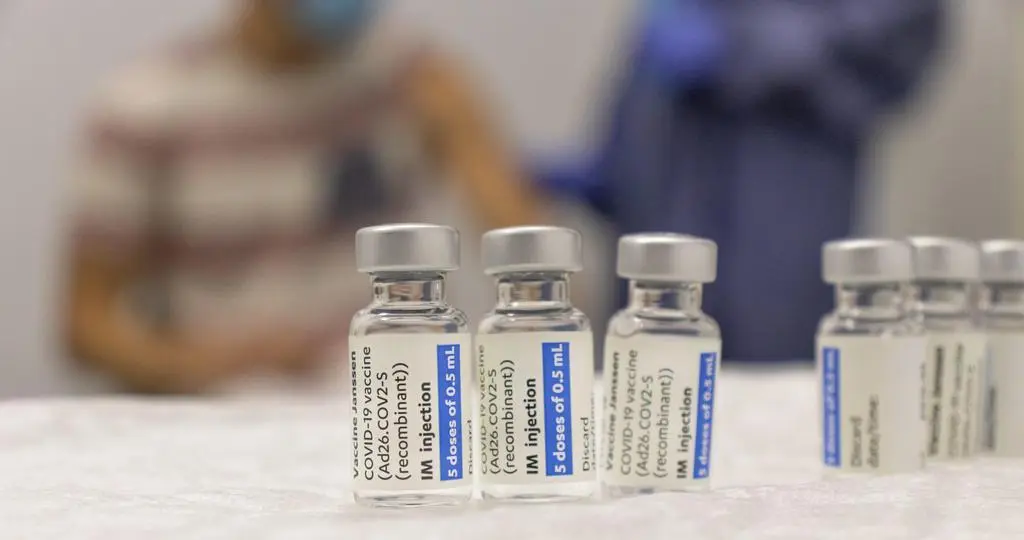
La farmacéutica Pfizer y su socio alemán BioNTech han solicitado la licencia a la Agencia Europea del Medicamento para administrar la vacuna contra la Covid-19 al grupo de menores entre 5 y 11 años (excluido de los grupos etarios en Europa). Lo hace en un momento en el que EEUU ya prepara la campaña para la administración de la vacuna en esta franja de edad.
La solicitud llega tras los resultados de las últimas pruebas clínicas que revelan que la vacuna es altamente eficaz entre los niños de esta franja de edad, una documentación que ha presentado a la EMA junto a toda la documentación y análisis clínicos correspondientes a la espera del pronunciamiento del organismo. En EEUU, la farmacéutica solicitó la autorización hace ya una semana, si bien su presidente asegura que ya disponen del estocaje suficiente para iniciar la vacunación.
Pfizer ha sido la primera farmacéutica en solicitar la autorización de su vacuna contra el coronavirus en menores de 11 años al tiempo que ya fue en su día la primera en recibir el visto bueno a la administración de las dosis en adultos. En el caso del suero empleado para menores de 11 años, la dosis es tres veces menos -en el caso de las dos pautas- con respecto al suero empleado en mayores de 12 años.
En caso de que la EMA avalara el uso del suero de Pfizer/BioNTech en menores de 11 años se podría arrancar todo el proceso para que la vacunación estuviera lista a finales del mes de octubre o primeros de noviembre, según los cálculos de los expertos.